
1. UKCA标记的时间点
从2021年1月1日开始适用
从2023年7月1日起将设备投放到GB市场必须使用;但不适用于NI交易者。
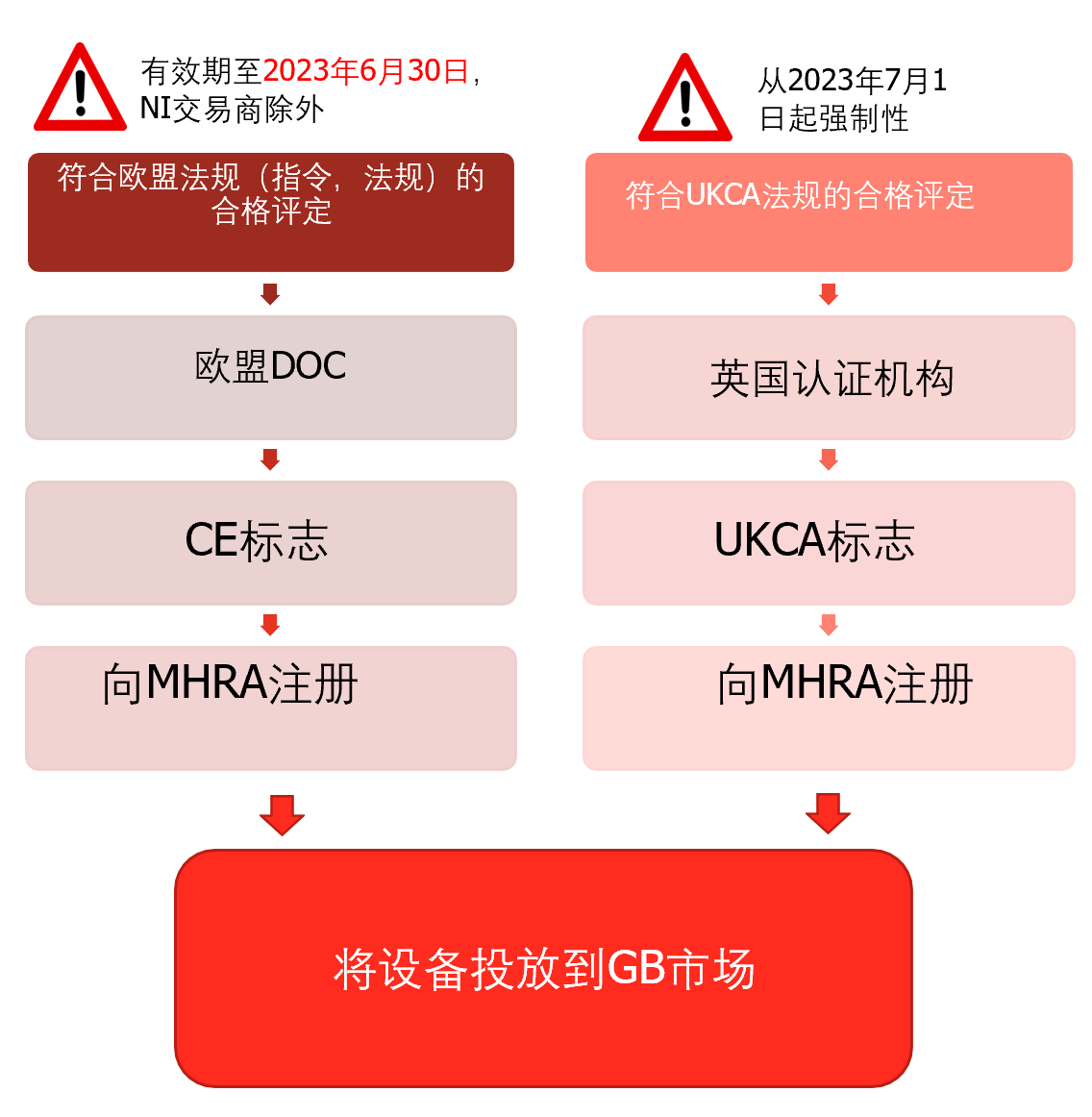
2. UKCA 的合格评定程序
由英国认可的认证机构开展UK MDR 2002的评审,合格后加贴UKCA标志。原则上原位于英国的MDD/IVDD的公告机构可以直接转换成英国认可的UK MDR 2002的认证机构,不需要额外的认可程序。
I类医疗器械和通用IVD的制造商将能够自行声明其是否符合UK MDR 2002的第二部分和第四部分(以2021年1月1日的形式存在),然后再贴上UKCA标记并放置该设备在英国市场上。
3. UKCA图片使用规则
您必须确保:
· 等比例调整图片大小;
· UKCA标记的高度至少为5mm-除非相关法律规定了不同的最小尺寸 ;
· UKCA标记清晰可见,清晰可见。

4. 加贴UKCA标记
在大多数情况下,您必须在产品本身或包装上使用UKCA标记。
在某些情况下,它可能放在手册或其他支持文献上。
这将根据适用于该产品的特定法规而有所不同。
以下一般规则适用:
· UKCA标记只能由您作为制造商或您的授权代表在产品上加贴;
· 贴上UKCA标记时,您对产品符合相关法规的要求承担全部责任 ;
· 您只能使用UKCA标记来表明产品符合英国相关法规;
· 您不得将可能会误解UKCA标记的含义或形式的任何标记或标志提供给第三方;
· 您不得在产品上附加影响UKCA标记的可见性,易读性或含义的其他标记;
· 除非法律有特殊要求,否则不得在产品上放置UKCA标记。






